返回
R-(+)-1,1'-联萘-2,2'-二酚
- 中文名称:
- R-(+)-1,1'-联萘-2,2'-二酚
- 中文别名:
- R-1,1'-联-2-萘酚;
(R)-(+)-1,1'-联(2-萘酚);
R-(+)-1,1’-联萘-2,2’-二酚;
(R)-(+)-2,2'-二羟基-1,1'-联萘;
(R)-(+)-1,1'-联-2-萘酚;
R-联萘酚
- 英文名称:
- (R)-(+)-1,1'-Bi-2-naphthol
- 英文别名:
- (R)-(+)-1,1'-Bi-2-naphthol;
(R)-(+)-1,1'-Binaphthalene-2,2'-diol;
(R)-(+)-2,2'-Dihydroxy-1,1'-dinaphthyl;
(R)-(+)-1,1-Bi(2-Naphthol);
2,2'-DINAPHTHOL;
(R)-(+)-1,1'-Bi-2-naphtho;
Dihydroxydinaphthylwhitepowder;
BI-2-NAPHTHOL;
(S)-(+)-1,1'-binaphthyl-2,2'-diol;
(R)-(+)-BINOL;
(R)-(+)-1,1'-Bi(2-naphthol);
DI-B-NAPHTHOL;
(R)-[1,1'-Binaphthalene]-2,2'-diol;
(R)-(+)-2,2'-Dihydroxy-1,1'-binaphthyl;
(R)-(+)-1,1‘-Bi-2-naphthol
- CAS No.:
- 18531-94-7
- 分 子 式:
- C20H14O2
- 分 子 量:
- 286.33
- 精确分子量:
- 286.09900
- PSA:
- 40.46000
- MDL:
- MFCD00004068
- EINECS:
- 210-014-0
- BRN:
- 3616837
- InChI:
- The Key: PPTXVXKCQZKFBN-UHFFFAOYSA-N3
- 危险品标志:

- 风险术语:
- R36/37/38
- 安全术语:
- S24/25
- 分子结构式:
-
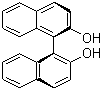
- SDS:
- 查看
推荐供应商
湖北云镁科技有限公司
R-1,1'-联-2-萘酚
- 联系人:方经理
- 电 话:027-59206672
- 手 机:18327059871
- Cas号:18531-94-7
- 包装:1kg铝箔袋/氟化瓶,10kg铝听/纸箱,25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:1.0元 - 25.0元
湖北诺纳科技有限公司
R-1,1'-联-2-萘酚
- 联系人:张经理
- 电 话:027-59209883
- 手 机:17386169806
- Cas号:18531-94-7
- 包装:1kg铝箔袋/氟化瓶,10kg铝听/纸箱,25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:1.0元 - 25.0元
湖北万得化工有限公司
R-(+)-1,1'-联萘-2,2'-二酚
- 联系人:王念
- 电 话:027-59210159
- 手 机:15172311821
- Cas号:18531-94-7
- 包装:1kg铝箔袋/氟化瓶,10kg铝听/纸箱,25kg纸板桶/编织袋/塑料桶,200kg镀锌铁桶/塑料桶,1t吨袋
- 纯度:99%
- 价格:1.0元 - 1,000.0元
湖北齐飞医药化工有限公司
R-1,1'-联-2-萘酚
- 联系人:汪军蕊(微信同号)
- 电 话:027-59322506
- 手 机:18071128683
- Cas号:18531-94-7
- 包装:25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:25.0元
湖北信康医药化工有限公司
(R)-(+)-1,1''-联萘-2,2''-二酚
- 联系人:张经理
- 电 话:027-59308705
- 手 机:18827031272
- Cas号:18531-94-7
- 包装:25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:25.0元
天门恒昌化工有限公司
R-1,1'-联-2-萘酚
- 联系人:黄湘迪
- 电 话:027-59322316
- 手 机:15827039378
- Cas号:18531-94-7
- 包装:25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:25.0元
湖北永阔科技有限公司
R-1,1'-联-2-萘酚
- 联系人:黄蓉
- 电 话:027-59223108
- 手 机:15107166787
- Cas号:18531-94-7
- 包装:25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:25.0元
湖北实顺生物科技有限公司
R-1,1'-联-2-萘酚
- 联系人:付经理
- 电 话:027-59223025
- 手 机:15107168801
- Cas号:18531-94-7
- 包装:25kg纸板桶/编织袋/塑料桶
- 纯度:99%
- 价格:25.0元
湖北广奥生物科技有限公司
R-(+)-1,1'-联萘-2,2'-二酚
- 联系人:付玉
- 电 话:027-59223056
- 手 机:15271829679
- Cas号:18531-94-7
- 包装:1kg铝箔袋/氟化瓶,10kg铝听/纸箱,25kg纸板桶/编织袋/塑料桶,200kg镀锌铁桶/塑料桶,1t吨袋
- 纯度:99%
- 价格:1.0元 - 1,000.0元





