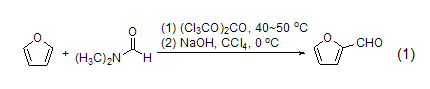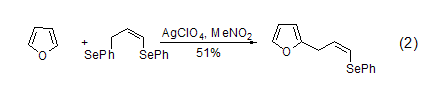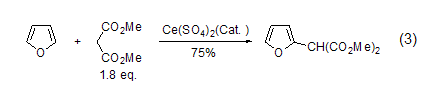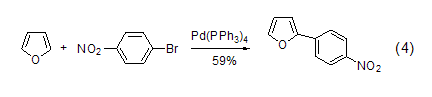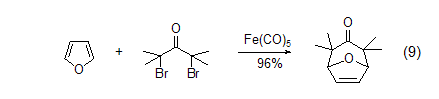1.呋喃是很好的富电芳香杂环,可与金属形成金属有机化合物参与反应,可发生[2+2]光反应、[2+3]环加成、[4+3]环加成和Diels-Alder反应,也可以发生卡宾反应[1]。
2-卤代、酰基、氰基、磺酰基和羰基呋喃的合成 呋喃作为富电的芳香杂环可以与很多的亲电试剂发生反应,用以制备卤代呋喃、酰基呋喃、氰代呋喃和其它杂原子取代呋喃等产物 (式1)[2]。一般情况下C-2位比C-3位更容易受亲电试剂的进攻。
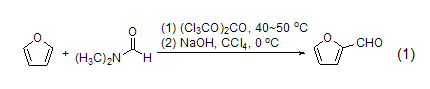
烷基呋喃的合成 烷基呋喃可由呋喃经过亲电取代反应制得。呋喃发生Mannich反应可生成2-(N,N-二烷基氨基)甲基呋喃衍生物,TMSI存在下呋喃也可以与β-酮发生反应。而在Ag+催化下,1,3-二苯基硒丙烷 (式2) 或者氯代环丙烷可与呋喃发生烯丙基化[3]。
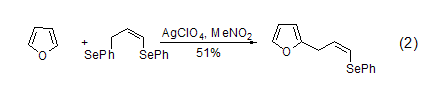
与游离基的反应 呋喃可以和亲电的碳游离基反应得到2-烷基取代的呋喃 (式3)[4]。
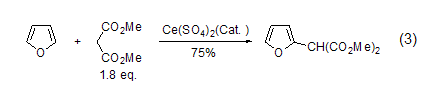
在Pd催化下,带有吸电子基团的溴化物与可以呋喃直接偶合 (式4)[5]。
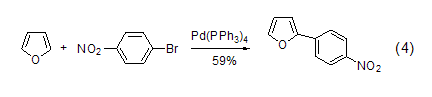
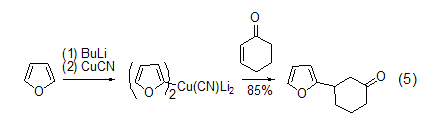
有机金属化合物 呋喃锂盐在有机合成中广泛使用。金属取代的呋喃可以与很多的亲电试剂发生反应,而且2-锂代呋喃也可以发生金属的转移反应。2-取代呋喃的高价铜酸盐可以在低温下与酮发生共轭加成反应 (式5)[6]。
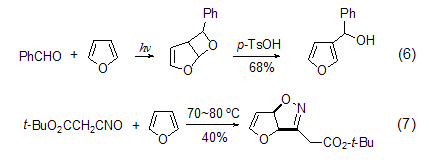
烯的环加成 光照下羰基化合物与呋喃[2+2]环加成生成环醚后,用酸处理可得到3-取代呋喃 (式6)[7]。呋喃与氰氧化物会发生[2+3]环加成 (式7),可用来合成多羟基胺类化合物[8]。
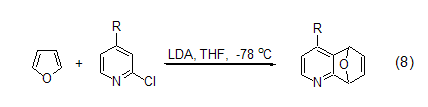
二烯的环加成 呋喃以二烯的形式参与Diels-Alder反应是呋喃在有机合成中最广泛的应用,提供了很多碳碳键的形成方法并可用于后续的合成。但是由于呋喃本身的芳香性,Diels-Alder反应速度都很慢。呋喃不仅能与丙二烯化合物发生Diels-Alder反应得到选择性的产物,而且还能和乙炔类化合物反应。呋喃和不同芳香烯的反应是合成多烯化合物的一种很好方法 (式8)[9]。
呋喃和偶极物质反应得到8-氧-二环[3.2.1]癸-6-烯-3-酮 (式9)[10]。这些[4+3]的环加成产物能很容易地转变成环庚酮、环庚三烯酮以及被取代的环庚烷体系,或是被取代的四氢呋喃化合物。
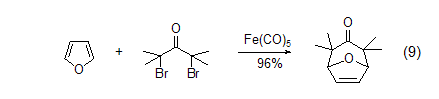
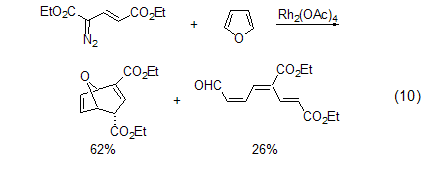
卡宾反应 包括卡宾加成生成2-氧-二环[3.1.0]己-3-烯的反应等。呋喃与乙烯基卡宾反应会得到两种产物 (式10)[11,12]。
2.稳定性[33] 稳定
3.禁配物[34] 强氧化剂、酸类
4.避免接触的条件[35] 空气
5.聚合危害[36] 不聚合
1.性状:无色液体,有温和的香味。[13]
2.熔点(℃):-85.6[14]
3.沸点(℃):31.4[15]
4.相对密度(水=1):0.94[16]
5.相对蒸气密度(空气=1):2.35[17]
6.饱和蒸气压(kPa):65.6(20℃)[18]
7.燃烧热(kJ/mol):-2090.4[19]
8.临界压力(MPa):5.32[20]
9.辛醇/水分配系数:1.34[21]
10.闪点(℃):-35(CC)[22]
11.引燃温度(℃):390[23]
12.爆炸上限(%):14.3[24]
13.爆炸下限(%):2.3[25]
14.溶解性:不溶于水,溶于丙酮、苯,易溶于乙醇、乙醚等多数有机溶剂。[26]
15.折射率(n20ºC):1.4214
16.蒸发热(J/mol,31.2ºC):399.8
17.生成热(KJ/mol):62.0
18.相对密度(20℃,4℃):0.9514
19.临界密度(g·cm-3):0.312
20.临界体积(cm3·mol-1):218
21.临界压缩因子:0.294
22.偏心因子:0.200
23.溶度参数(J·cm-3)0.5:18.541
24.van der Waals面积(cm2·mol-1):4.920×109
25.van der Waals体积(cm3·mol-1):37.580
26.气相标准燃烧热(焓)(kJ·mol-1):-2110.95
27.气相标准声称热(焓)( kJ·mol-1) :-34.73
28.气相标准熵(J·mol-1·K-1) :267.25
29.气相标准生成自由能( kJ·mol-1):0.9
30.气相标准热熔(J·mol-1·K-1):65.40
31.液相标准燃烧热(焓)(kJ·mol-1):-2083.30
32.液相标准声称热(焓)( kJ·mol-1):-62.38
33.液相标准熵(J·mol-1·K-1) :176.95
34.液相标准生成自由能( kJ·mol-1):0.17
35.液相标准热熔(J·mol-1·K-1):114.56
 F+
F+ T
T
 F+
F+ T
T