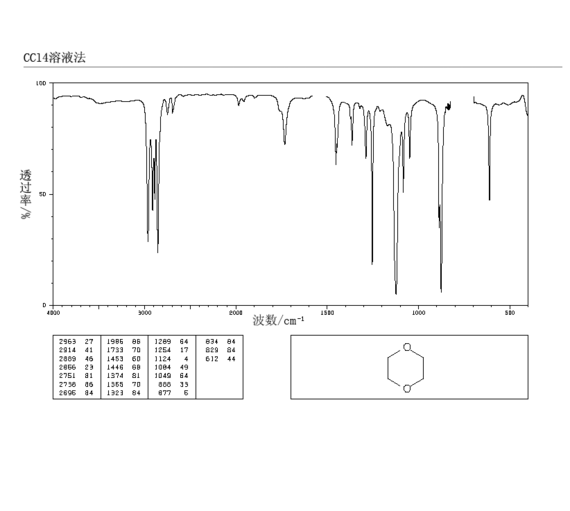
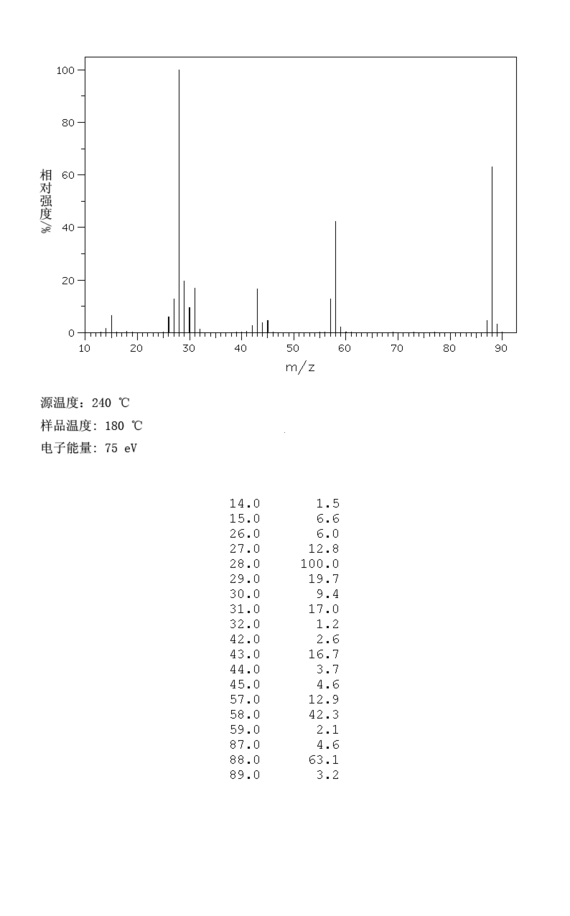
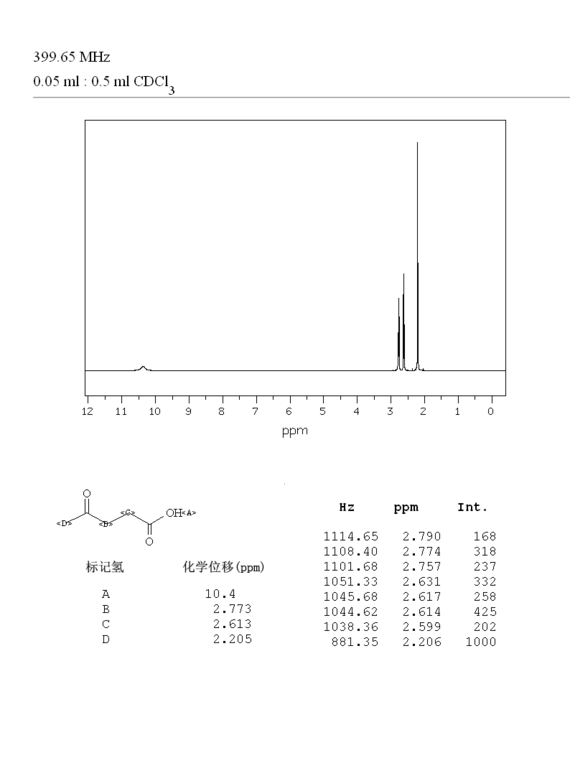
1.化学性质:与一般的饱和醚相似,是比较稳定的化合物。在空气中氧的作用下,特别在散射光照射时,形成有爆炸性的过氧化物。对碱、金属钠和弱酸稳定。强酸、强氧化剂在高温、高压下使醚键破裂而开环。与卤化氢作用时,生成1,2-二卤代乙烷和乙二醇。加热时与浓硫酸作用生成2-甲基-1,3-二戊烷等。
2.与乙酸或乙酐在加热时作用,生成乙二醇二乙酸酯。能与卤素、硝酸、硫酸以及其他无机化合物形成络合物。例如与卤素形成C4H8O2Br2(m.p. 66℃)、C4H8O2I2(m.p. 84℃)、C4H8O2Cl2,与硫酸形成C4H8O2H2SO4(m.p. 101℃)等氧化合物。与氯化锂或三氟化硼也能形成络合物LiCl·C4H8O2·H2O,BF3·2H2O·C4H8O2。在钯、铑、镍等金属催化下,二噁烷在重氢和醚间进行同位素交换。二噁烷与四硝基甲烷反应呈鲜黄色,此反应可用来检验二噁烷。
3.属微毒类。毒性比乙醚强2~3倍。中毒时最初出现麻醉、呕吐,尿频后尿减少,终至停止排尿。同时血液中尿素增加,嗜眠,昏睡,2~3日后死亡。长期接触或吸入其蒸气时,刺激眼、鼻、咽喉和肺,损害肝、肾、脑和皮肤。工作场所最高容许浓度360mg/m3,超过720mg/m3时即能引起头痛和胃痛等症状。二噁烷能经皮肤吸收而中毒,接触皮肤时应用大量水冲洗和用肥皂洗净。
4.稳定性[25] 稳定
5.禁配物[26] 强氧化剂、强还原剂、卤素
6.避免接触的条件[27] 光照,接触空气
7.聚合危害[28] 不聚合
1.性状:无色,带有醚味的透明液体。[1]
2.熔点(℃):11.8[2]
3.沸点(℃):101.3[3]
4.相对密度(水=1):1.04[4]
5.相对蒸气密度(空气=1):3.03[5]
6.饱和蒸气压(kPa):4.1(20℃)[6]
7.燃烧热(kJ/mol):-2428.6[7]
8.临界温度(℃):312[8]
9.临界压力(MPa):5.14[9]
10.辛醇/水分配系数:-0.27[10]
11.闪点(℃):12(CC);18.3(OC)[11]
12.引燃温度(℃):180[12]
13.爆炸上限(%):22.2[13]
14.爆炸下限(%):2.0[14]
15.溶解性:与水混溶,可混溶于多数有机溶剂。[15]
16.折射率(n20ºC):1.4229
17.折射率(n25ºC):1.4203
18.黏度(mPa·s,20ºC):1.3
19.黏度(mPa·s,25ºC):1.2
20.黏度(mPa·s,30ºC):1.087
21.闪点(ºC,闭口):12.2
22.闪点(ºC,开口):15.6
23.燃点(ºC):180
24.蒸发热(KJ/mol):35.80
25.熔化热(KJ/mol):12.5
26.比热容(KJ/(kg·K),20ºC):1.72
27.电导率(S/m,25ºC):<2×10-8
28.体膨胀系数(K-1,20ºC):0.001030
29.体膨胀系数(K-1,0~55ºC):0.001070
30.体膨胀系数(K-1,55ºC):0.00113
31.相对密度(25℃,4℃):1.0281
32.临界密度(g·cm-3):0.37
33.临界体积(cm3·mol-1):238
34.临界压缩因子:0.254
35.偏心因子:0.280
36.溶度参数(J·cm-3)0.5:20.163
37.van der Waals面积(cm2·mol-1):5.900×109
38.van der Waals体积(cm3·mol-1):46.620
39.气相标准燃烧热(焓)(kJ·mol-1):-2400.9
40.气相标准声称热(焓)( kJ·mol-1) :-315.3
41.气相标准熵(J·mol-1·K-1) :299.66
42.气相标准生成自由能( kJ·mol-1):-180.8
43.气相标准热熔(J·mol-1·K-1):92.18
44.液相标准燃烧热(焓)(kJ·mol-1):-2362.2
45.液相标准声称热(焓)( kJ·mol-1):-355.1
46.液相标准熵(J·mol-1·K-1) :195.27
47.液相标准生成自由能( kJ·mol-1):-189.7
48.液相标准热熔(J·mol-1·K-1):150
 F
F Xn
Xn
 F
F Xn
Xn